肝星状细胞激活过程中胞外囊泡功能和蛋白质组的动态变化

肝纤维化是慢性肝损伤的结果,其特征是胶原蛋白和其他不溶性细胞外基质成分的沉积。肝脏中引起纤维化的主要细胞是位于窦间隙的肝星状细胞(HSC)。正常情况下,星状细胞是静止的周细胞样细胞。然而,在肝损伤时星状细胞表型激活,成为可收缩的胶原从而生成肌成纤维细胞。在急性损伤条件下会产生临时基质来支持肝细胞的再生。在慢性损伤条件下则会持续不断地产生纤维化物质,进而形成瘢痕并使受损的肝功能进一步恶化。肝纤维化是导致发病和死亡的主要原因,也是导致肝硬化的重要因素。星状细胞的生物活性是其与肝脏其他细胞协同作用的结果。

最近研究发现了新的肝脏信号网络,主要是通过胞外囊泡(EVs)实现不同肝细胞之间的信息传递。EV是一种微小的膜结构(50-500nm),人们对其内部运载的物质与分泌来源的表型之间的规律越来越感兴趣。本研究通过比较激活状态及非激活状态的HSC细胞外泌体内蛋白质的比较分析,发现这些蛋白质在两种细胞中的功能和分子荷载均呈现显著差异。作者也比较了鼠源和人源激活状态下HSC EVs内的蛋白质,发现两者之间的蛋白成分和预测功能均高度相似。
方法与结果
1.HSC细胞特征性描述
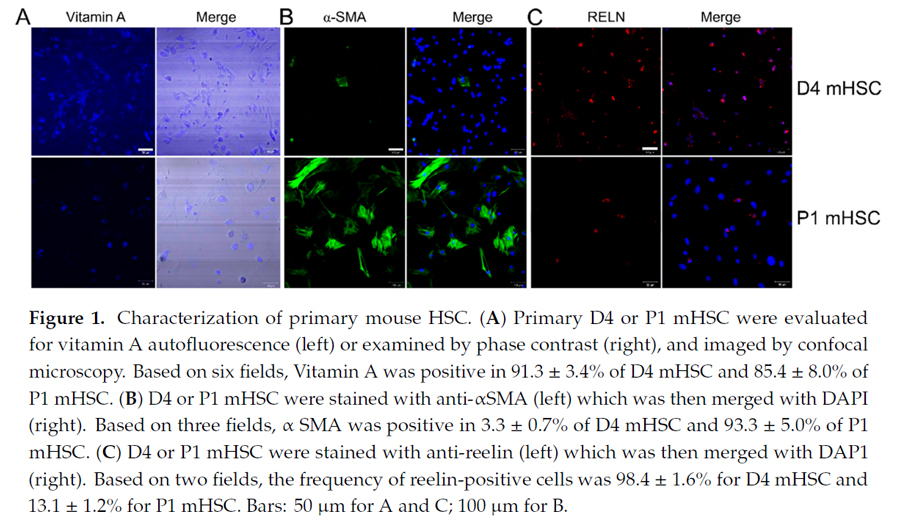
利用储存在HSC内胞质油滴中维生素A的自体荧光特性,来评估HSC细胞(如图1A)。而αSMA是HSC被激活的标志(图1B)。RELN代表着未被激活的HSC(图1C)。实验结果呈现了D4为相对P1静止的细胞状态。确保细胞的状态为后续EVs的分离和分析垫定基础。
2.人源和鼠源HSC EVs的物理化学和生物特性
激活状态下的鼠源HSC分泌的EVs数量是未激活状态下的4.5倍。通过NTA,WB及qRT-PCR技术,对人源HSC(hHSC),鼠源HSC(mHSC)的EVs进行了评估。
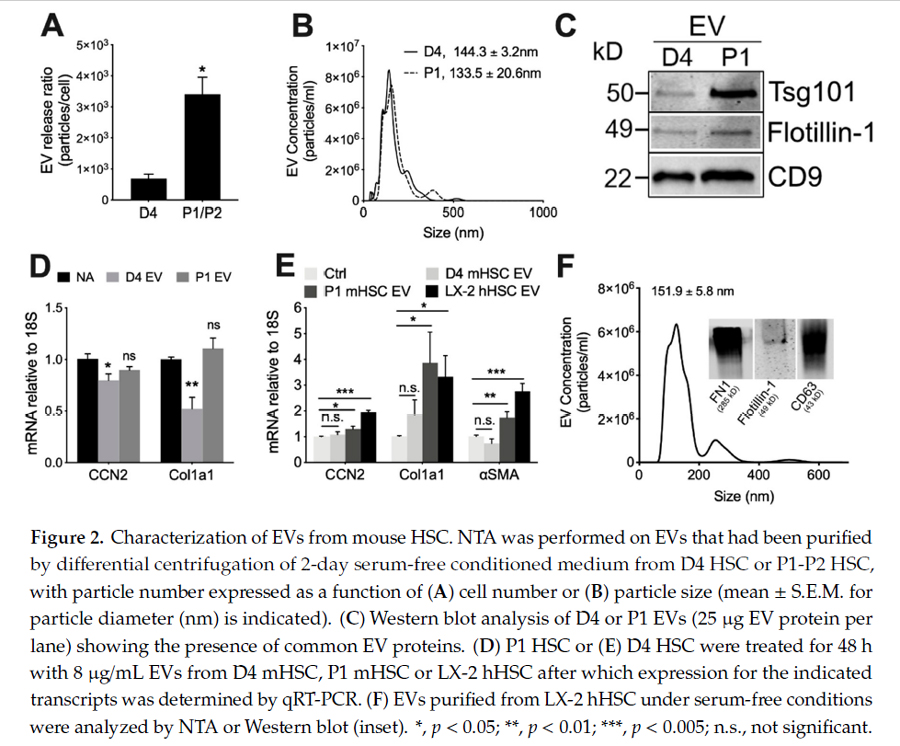
3.mHSC EVs蛋白质组学分析, Western blot及qRT-PCR验证。
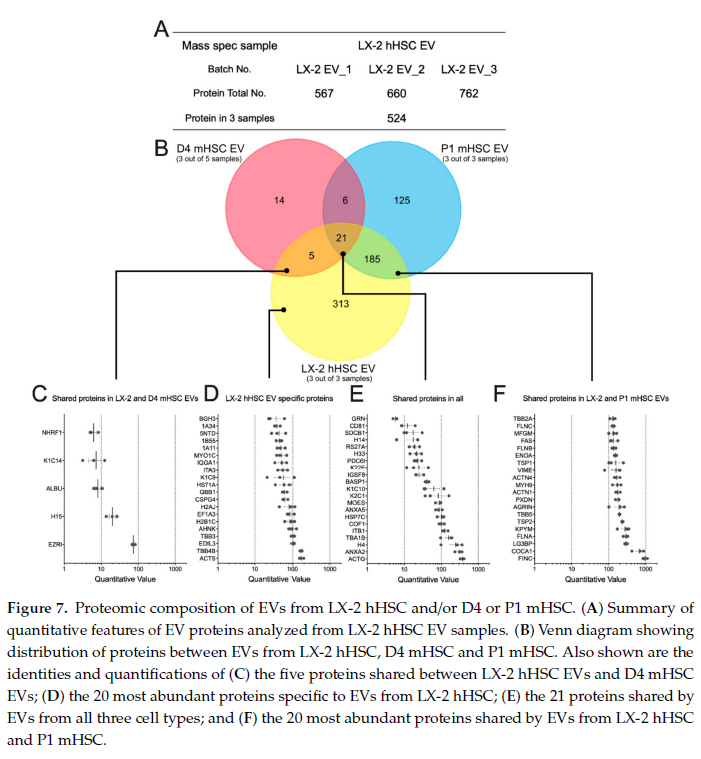
D4 mHSC EVs中共鉴定到46种蛋白质,其中组蛋白和胶质蛋白占主体,而P1 mHSC中鉴定到337种蛋白质,与细胞外空间或基质、蛋白酶体、胶原蛋白、囊泡运输、代谢酶、核糖体和伴侣蛋白相关。并通过WB及qRT-PCR技术对蛋白质组学结果进行验证。

4.hHSC EVs蛋白质组学分析
P1 LX-2HSC (hHSC)细胞系的EVs在体外也促进了D4 mHSC的成纤维基因表达,共鉴定到524个蛋白,通过GO和KEGG等生物信息学分析发现鉴定到的许多蛋白与P1 mHSC EVs是同种蛋白或具有相同的生物学功能。
结论
mHSC的激活与EV产量的增加相关,也与EV生物活性相关。即EV介导的mHSC成纤维基因表达的抑制让位于EV介导的mHSC成纤维基因表达的刺激,并显著增加了EV蛋白组的复杂性。活化的hHSC产生的EVs表现出纤维化活性,并具有与活化的mHSC EVs相似的蛋白成分和功能。因此,我们认为HSC激活引起的EVs的产生、功能和蛋白含量的变化可能有助于HSC在体内的功能调节和肝纤维化通路的微调。
文章亮点
利用蛋白质组学技术研究肝损伤过程中胞外囊泡蛋白质组分和功能的变化,从而发掘肝纤维化相关通路的调控机制。
参考文献
Li X, Chen R, Kemper S, Brigstock DR. Dynamic Changes in Function and Proteomic Composition of Extracellular Vesicles from Hepatic Stellate Cells during Cellular Activation. Cells. 2020;9(2):290. Published 2020 Jan 25. doi:10.3390/cells9020290
